От сбалансированности элементов в составе кровяной жидкости зависит правильность работы всех систем человеческого тела. Если концентрация какого-либо из них нарушается, это становится причиной сбоя в
Читать далее

От сбалансированности элементов в составе кровяной жидкости зависит правильность работы всех систем человеческого тела. Если концентрация какого-либо из них нарушается, это становится причиной сбоя в
Читать далее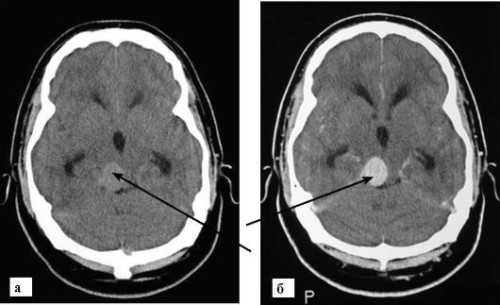
Повторный инсульт чаще происходит у людей с артериальной гипертензией, аритмией, сахарным диабетом. Вероятность второй катастрофы возрастает при отсутствии лечения, физически неактивном образе жизни. Однако атаку
Читать далее
Излечившись от инсульта один раз, при полноценном восстановлении функций организма пациент со временем прекращает уделять здоровью надлежащее внимание, думая, что рецидива произойти не может. На
Читать далее
Минеральная добавка. Применение: острый инфаркт миокарда, тахикардия, сердечная недостаточность. Цена от 161 руб. Аналоги: Рибоксин, Кардиомагнил, Аспаркам. Что за препарат Панангин таблетки – минеральная добавка,
Читать далее
Актуальность инсультов головного мозга в мире очень высока: инсульты делят с инфарктами миокарда первое место среди причин смертности населения. Воспаление легких как осложнение после инсульта
Читать далее