Человеческий организм — чрезвычайно сложная конструкция, в ней имеется множество разнообразных взаимосвязанных между собой биологических систем, каждая из которых отвечает за жизненно важный элемент этой самой конструкции.
Для примера рассмотрим систему гемостаза. Ее предназначение — в сохранении крови в состоянии жидкости. Но если в результате травмы стенок сосуда возникнет кровотечение — система гемостаза немедленно отреагирует и направит свою работу на остановку кровотечения.
После успешного ее завершения система гемостаза создаст условия для растворения тромбов — они уже выполнили свою работу и более не должны находиться в кровеносной системе.
Содержание
Что такое первичный гемостаз
Клетки крови, которые отвечают за функцию свертывания:
- тромбоциты,
- плазменные факторы свертывания и их ингибиторы.
За процесс гемостаза отвечают такие структурные компоненты:
- Стенки кровеносных сосудов
- Кровяные клетки
- Плазменно-ферментные системы
Гемостаз представляет собой нераздельно совмещенные системы. Его работа осуществляется под воздействием нейрогуморального регулирования. В этой системе безупречно работают механизмы отрицательной и положительной связи, именно это дает возможность быстрого создания сгустка, и после — моментального его растворения.
Неразрывно совмещены между собой работа внутренней оболочки кровеносных сосудов и тромбоцитов, они вместе создают механизм который зовется — первичный сосудисто-тромбоцитарный гемостаз.
Первичный тромбоцитарный гемостаз являет собою ряд реакций, главная функция которых заключается в том чтобы уменьшить или прекратить кровопотерю. Первичный гемостаз отвечает за остановку крови сразу после ушиба капилляров, в течение первых двух-трёх минут.
Этапы сосудисто-тромбоцитарного гемостаза
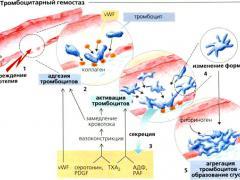
Сосудисто-тромбоцитарный гемостаз подразделяют на следующие этапы. Первой реакцией сосуда на повреждение является спазм, продолжительность которого не превышает 1 минуту, а сужение просвета сосуда может достигать трети его изначального диаметра.
На сегодня медицина не имеет однозначного мнения по поводу механизма спазма сосуда. Предполагается, что он — результат нейрогенного воздействия, сопровождающегося выделением серотонина и тромбоксана из тромбоцитов, которые были активированы.
Процесс адгезии реализуется в результате приобретения стенкой сосуда положительного заряда. Поскольку заряд тромбоцитов отрицателен, то они скапливаются вблизи точки ранения. Их форма изменяется, они приобретают удлиненную форму и контактируют с соединительными тканями стенок сосудов.
Далее происходит агрегация тромбоцитов.
Она разделена на несколько фаз:
- Обратная — заключающаяся в образовании неплотного тромбоцитарного сгустка, на этот процесс оказывают влияние физиологически активные вещества. Плазма свободно проникает сквозь образовавшийся сгусток.
- На фазе необратимой агрегации происходит образование плотного гомогенного тромбоцитарного сгустка более крупных размеров. Наступление этой фазы связано с освобождением содержимого тромбоцитарных гранул. Отличительная характеристика сгустка — неспособность пропускать плазму.
Далее происходит уплотнение тромба, образованного тромбоцитами.
Нарушения в течении упомянутых стадий может закончиться возникновением кровотечения.
Нарушение баланса в выработке тромбоцитов грозит развитием заболеваний и патологических состояний, в частности — если тромбоцитов слишком мало, то о качественной адгезии говорить не приходится, ведь компоненты для склеивания отсутствуют.
Адгезия формирует тромб, который, даже при довольно сильном потоке крови, не даст погибнуть человеку. Но когда количество тромбоцитов слишком большое они могут увеличиваться в размере, отрываться и перемещаться по кровеносным сосудам, это очень нежелательное и опасное явление.
К сожалению, бывают патологии, при которых факт тромбообразования совсем нежелателен — он может нарушить процесс питания жизненно важных органов (при инсульте, инфаркте миокарда). Агрегация испытывает патологические изменения, медикам приходится разрабатывать схему применения различных лекарственных средств.
Выделение биологически активных веществ, происходит при освобождении тромбоцитов:
- АДФ
- Серотонин
- Адреналин
- Простагландины
- Тромбоксаны А2
Эти вещества стимулируют агрегацию остальных тромбоцитов, которые мгновенно выходят из кровотока, а потом фиксируются на агрегированных тромбоцитах, в следствии формируется тромбоцитный агрегат.
Вторичный (коагуляционный) гемостаз
Связь между первичным и вторичным гемостазом просматривается достаточно четко.
Коагуляционный гемостаз длится пару минут, по сути является реакцией, происходящей между плазменными белками, в результате которой происходит формирование фибриновых нитей.
Этот процесс приводит к прекращению кровотечения из поврежденного сосуда и предотвращает возобновление кровотечения по истечению некоторого времени.
Далее происходит сжатие кровяного сгустка, образованного в результате вторичного гемостаза, т.е. происходит ретракция. Завершается процесс образованием гемостатической пробки, которая в результате сокращения кровяного сгустка приобретает большую плотность. Наступает полная остановка кровотечения.
Ряд реакций которые происходят при свертывании ведут к окончанию создания тромбина и его количества вполне достаточно для того чтобы часть фибриногена преобразовалась в фибрин.
Вторичный гемостаз может активироваться двумя механизмами.
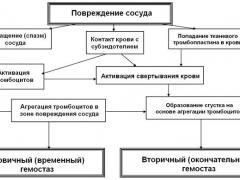
Внешний
Происходит когда в кровь попадает тканевый тромбопластин. Началом этого процесса является контакт коллагена с фактором свертывания на месте травмированного сосуда.
Внутренний
Когда из внешней среды не попадает тромбоплатин, этот процесс запускают тканевые факторы.
Когда начинает действовать внешний механизм, то фактор ІІІ начинает взаимодействовать с фактором VII и тут же начинает активироваться фактор Х. Уже активированный фактор Х совместно с фактором V (это фосфолипидный фактор) вырабатывают протромбин.
А при действии внутреннего механизма начинают работать факторы ХІІ, ХІ, ІХ, VIII, вместе с факторами X, V которые принимают участие и у внешнем механизме. Данный механизм начинает действовать, когда изменяется состояние сосудистой стеки.
В момент прикосновения крови до поврежденной части сосуда начинает активизироваться фактор ХІІ, который в свою очередь начинает переводить в активное состояние фактор ХІ. В активном состоянии он воздействует на фактор ІХ и такая сцепная активация всех факторов способствует образованию тромбокиназы.
Внутренний и внешний механизмы неразрывно связанны между собою. Такую связь обеспечивают калликреины кинины, они являют собою белковые вещества.
Тромбин образовывается на второй фазе, путем расщепления молекул протромбиназа на части, одна из этих частей с помощью фактора Ха превращается в тромбин.
Третья фаза заключается в том, что образовывается фибрин который есть основою сгустка. Фактор ХІІІа приводит к стабилизации молекул фибрина и участвует в образовании глютамин-лизиновых связей между молекулами фибрина.
На четвертой фазе (посткоагуляционной) происходят процессы уплотнения, сжатия и растворения сгустка.
Как только фибриновый тромб образовался сразу же начинается такой процесс как фибринолиз – во время которого растворяется тромб и сгустки крови.
Свертывание крови работает очень слаженно, даже небольшая частица факторов свертывания мгновенно образует активную форму. Именно это не позволяет тромбу распространиться за область поврежденной части сосуда.
Для организма очень важна слаженная работа этого процесса потому что способность свертывания 1 миллилитра крови может привести к свертыванию за 15 секунд всего фибриногена, который есть в организме.
Исследование гемостаза
Когда проводят оценку свертываемости крови, в обязательном порядке собирают анамнез, больному могут задать ряд вопросов таких как:
- Были ли у пациента случаи переливания крови?
- Сталкивался ли пациент с необъяснимо сильными кровотечениями при хирургических вмешательствах?
- Возможно были у больного кровотечения при небольших операциях?
- Били ли неожиданные кровоизлияния?
- Страдал ли кто-то из родственников такой проблемой?
Перед тем как собрать анамнез медики исследуют пациента на наличие различных заболеваний, которые могли повлиять на процесс гемостаза.
Исследование гемостаза в лаборатории заключается в изучении количества тромбоцитов. Тромбоцитопения — это понижение уровня тромбоцитов.
Причинами ее возникновения могут бить:
- Инфекции
- Миелодисплазия
- Радиация
- Дефицит В12
- Миелопролиферативное заболевание
Спонтанно могут возникнуть если кровь содержит много тромбоцитов. Они могут возникнуть и когда функция тромбоцитов работает не правильно, изъяны тромбоцитов оценивают при исследовании агрегации.
К веществам которые подавляют функцию тромбоцитов относят:
- Гепарин
- Аспирин
- Алкоголь
- НПВС
- Употребление в больших количествах пенициллина
В большинстве случаев ухудшению функций тромбоцитов способствуют совмещение употребления аспирина и алкоголя одновременно. После употребления всех выше перечисленных веществ должно пройти как минимум двадцать четыре часа чтобы функция тромбоцитов возобновилась.
Возобновление тромбоцитов происходит ежедневно, в пределах от двадцати до тридцати процентов, он если говорить про воздействие аспирина то следует помнить, что аспирин ухудшает функции тромбоцитов навсегда.
В ходе исследования системы гемостаза особое внимание уделяют процессу образования тромбов. Повышение уровня тромбоцитов исследуют смотря на разные отрасли в медицине. Эмбология тромбов может стать причиной большого количества мозговых импульсов, инфаркт миокарда может случиться в случаи тромбозов коронарных сосудов.
Также может возникнуть угроза ампутации нижней конечности при закупорке основных артерий конечностей. Некроз кишечника случается в случае когда у больного появляется венозный и артериальный тромбоз в артериальных сосудах.
- Более наглядно о первичном гемостазе — на видео:
Взаимодействие тромбоцитов и сосудистой стенки
В кровотоке постоянно содержится от 20 до 40% активированных «дежурных» тромбоцитов, готовых при появлении молекул адгезии моментально начать процесс свертывания крови. В процессе тромбоцитарно-сосудистого взаимодействия различают стадии адгезии тромбоцитов, их активации и агрегации.
Адгезия
При повреждении стенки сосуда обнажается коллаген базальной мемраны и создается чужеродная «тромбогенная» контактная поверхность, одновременно из активированного эндотелия высвобождаются белки адгезии, в первую очередь фактор Виллебранда. Контактная поверхность адгезирует тромбоциты и запускает процесс свертывания.
Процесс адгезии заключается в прикреплении тромбоцитов, оказавшихся в зоне повреждения, к субэндотелиальным структурам.
При этом происходит прямой контакт тромбоцитов и коллагена базальной мембраны через тромбоцитарные рецепторы GPIa/IIa. Одновременно выделенный из поврежденных эндотелиоцитов ф.
Виллебранда связывается одной своей частью с тромбоцитарным рецептором GPIb, а другой – с коллагеном субэндотелия.
Адгезия тромбоцитов
После прикрепления к поврежденной поверхности тромбоциты активируются.
Активация
Адгезия тромбоцитов к коллагену (рецепторы GPIa/IIa) и взаимодействие с фактором Виллебранда (рецептор GPIb) приводит к их активации.
Связывание фактора Виллебранда с рецептором GPIb запускает фосфолипид-кальциевый механизм передачи сигнала, что, в конце концов, приводит к повышению внутриклеточной концентрации ионов Cа2+ и активации протеинкиназы С. В результате:
- ингибируется АТФ-зависимая аминофосфолипид-транслоказа, поддерживающая мембранную асимметрию фосфолипидов, и в результате на наружной поверхности мембраны появляется отрицательно заряженный фосфатидилсерин.
- вместе с фосфатидилсерином на поверхность выходит особый гликопротеин (тканевой фактор), формируется комплекс тканевого фактора. Мембрана становится поверхностью для взаимодействия плазменных факторов свертывания, которая также называется тромбоцитарный тромбопластин.
- происходит сокращение белка тромбостенина, в результате происходит дегрануляция и наружу высвобождаются факторы, активирующие адгезию и агрегацию,
- изменяется форма тромбоцита, появляются псевдоподии, и он распластывается на контактной поверхности,
Процессы, происходящие при активации тромбоцита
- происходит активация фосфолипазы А2, которая от фосфатидилхолина мембраны отщепляет полиненасыщенную (например, арахидоновую) кислоту и из нее синтезируется тромбоксан А (например, тромбоксан А2) – сильный индуктор агрегации тромбоцитов и вазоконстриктор. Тромбоксан противодействует влиянию простациклинов, препятствуя активации аденилатциклазы и прерывая эффекты простациклинов.
Антагонизм действия простациклинов и тромбоксанов
Тромбоксан далее ускоряет высвобождение активных веществ (протромбина, PAF, АДФ, ионов Ca2+, серотонина, тромбоксана А и др.
) из активированного тромбоцита, что поддерживает и усиливает активацию этого и соседних тромбоцитов.
Активация усиливается также под действием АДФ, выделяющейся из поврежденных эритроцитов и эндотелиоцитов сосудистой стенки.
Уже активированные тромбоциты имеют на своей поверхности рецепторы для активных и неактивных факторов V, VIII, IX, X, XI, протромбина и тромбина.
Агрегация
Процесс агрегации заключается в стабилизации тромба фибрином и в слипании активированных тромбоцитов друг с другом.
Любой пусковой сигнал приводит в активированном тромбоците к конформационным изменениям рецептора GPIIb/IIIa, который перемещается на мембрану.
После связывания с этим рецептором фибриноген действует как мостик между прилегающими тромбоцитами и в зоне повреждения образуется тромбоцитарный тромб, армированный фибриногеном.
Поначалу связь между тромбоцитами еще не прочна и такая агрегация является обратимой. Активация и агрегация поддерживается непрерывной секрецией содержимого гранул из связывающихся тромбоцитов.
Продолжающаяся дегрануляция тромбоцитов и секреция ими простагландинов (PgG2 и PgH2), тромбоксана А2, АДФ, превращение фибриногена в фибрин (катализируемое тромбином) делают агрегацию необратимой. Такой тромбоцит прочно связан с другими клетками, он потерял содержимое гранул и не может вернуться в исходное состояние.
Агрегация тромбоцитов
Ретракция
Ретракция – это уплотнение сгустка крови с выделением из него избытка сыворотки. Стимулом для ретракции являются различные вещества, выделяемые тромбоцитом на этапах активации и агрегации.
Ретракция осуществляется благодаря тому, что к внутриклеточной части рецепторов GPIIb/IIIa присоединен сократительный белок тромбостенин (подобен актомиозину мышечных волокон), который при накоплении в цитозоле ионов Ca2+ сокращается и сжимает сгусток.
Сжатие сгустка обусловливает повышение давления внутри тромбоцита и вызывает дополнительный выброс веществ из его гранул, что еще более усиливает ретракцию и окончательно уплотняет тромб. В норме кровотечение из мелких сосудов продолжается не более 5 минут.
Тромбоцитарно-сосудистый гемостаз
Кровь — это жидкая соединительная ткань. Гемостаз — комплекс молекулярно-клеточных механизмов, обеспечивающих способность циркулирующей крови оставаться жидкой и предупреждать ее потерю при повреждении сосудов путем формирования тромба.
Гемостаз зависит от тонкого и сложного взаимодействия по меньшей мере четырех функциональных систем:
- Сосудов
- Тромбоцитов
- Свертывания крови
- Фибринолиза.
В соответствии с определением составляющими тромбоцитарно-сосудистого гемостаза являются тромбоциты и сосуды.
Тромбоцитарные и сосудистые заболевания характеризуются петехиями и / или малыми экхимозами, кровоизлияниями в слизистые (например, кровотечение десен, желудочно-кишечные кровотечения, меноррагии).
Кровотечения немедленные и обильные из небольших разрезов. Немедленные кровотечения позволяют отличить тромбоцитарные нарушения от кровотечений при недостаточности белков свертывания крови — поздних кровотечений.
Нарушения в системе тромбоцитов могут быть количественными или качественными.
Сосудистая система и гемостаз
В норме кровь свободно течет по сосудистой системе, без присоединения клеток крови к стенке сосудов.
Тонкий слой эндотелиальных клеток, выстилающих внутреннюю поверхность различных сосудов, помогает поддерживать тромбо-резистентность поверхности.
При повреждении сосудов при травме или при заболеваниях эндотелиальные клетки и тромбоциты взаимодействуют с факторами свертывания крови с образованием тромба в месте повреждения.
Тромбоциты и гемостаз
В гемостазе тромбоциты выполняют, по крайней мере, три функции:
- В ответ на повреждение сосудов, тромбоциты активируются и инициируют формирование первичного гемостатического тромба,
- Фосфолипиды мембраны тромбоцитов (иногда называют тромбоцитарный фактор 3 или ТФ3) для каскада свертывания,
- Принимают участие в поддержании целостности сосудистого эндотелия в месте повреждения сосуда реализуется следующая последовательность реакций (рис.). Во-первых, тромбоциты прилипают (адгезируют) к открытому субэндотелиальному слою коллагена. Прилипанию тромбоцитов предшествует изменение их формы: клетки поврежденной ткани освобождают АДФ — мощный активатор тромбоцитов. Во-вторых, активированные тромбоциты освобождают ряд соединений в том числе аденозиндифосфат (AДФ). Освобожденный АДФ стимулирует другие тромбоциты к адгезии в ране, и, в-третьих, происходит, агрегация активированных тромбоцитов. При агрегации тромбоциты прилипают друг к другу и инициируют начало образования тромба. Наконец, в месте повреждения активируются белки свертывания крови, образуется фермент тромбин, который превращает растворимый белок свертывания фибриноген в нерастворимые нити фибрина, нити армируют агрегаты тромбоцитов и заканчивают формирование белого тромбоцитарного тромба.
- Тромб выполняет как минимум две функции: останавливает кровотечение и инициирует ремонт сосудов и заживление ткани.
Сосуды в тромбоцитарно-сосудистом гемостазе
В зависимости от функционального состояния эндотелий сосудистой стенки обладает анти- и прокоагулянтными свойствами, т.е предупреждает образование тромбов, поддерживает кровь в жидком состоянии или, напротив, индуцирует формирование тромбов.
Как часть тромбоцитарно-сосудистого гемостаза, антикоагулянтные свойства проявляет неповрежденный эндотелий благодаря его способности синтезировать и непрерывно продуцировать молекулы, которые прямо или косвенно предупреждают образование тромбов:
- мощный ингибитор активации тромбоцитов простациклин,
- оксид азота (NO) – синергист простациклина,
- эндотелины – факторы расширяющие сосуды и замедляющие скорость кровотока;
- тканевый активатор плазминогена (t-PA);
- 13-гидроксиоктадекадиеновая кислота (13-НОДЕ) – ингибитор экспрессии рецепторов адгезии на поверхности эндотелиальных клеток;
- тромбомодулин (ТМ) – мембранный гликопротеин, связывающий тромбин;
- гепарин – ингибитор тромбина и реакций его образования;
- ингибитор сериновых протеаз НЕКСИН.
Поврежденный эндотелий (травмы, воспаления, аутоиммунная патология, гипоксия, инфекции и др.) проявляет прокоагулянтные свойства, которые в тромбоцитарно-сосудистом гемостазе реализуются:
- потерей, сбросом в кровоток тромбомодулина;
- синтезом тканевого тромбопластина;
- синтезом и секрецией ингибитора тканевого активатора плазминогена (PAI-1);
- секрецией фактора Виллебранда – VIII:WF;
- активацией тромбоцитов обнажившимся вместе повреждения сосудистой стенки коллагеном
Фактор Виллебранда играет важную роль в в тромбоцитарно-сосудистом гемостазе: фактор Виллебранда связывает субэндотелиальный коллагеновый матрикс и рецептор на тромбоцитах GP Ib-IX-V и, таким образом, обеспечивает прикрепление тромбоцитов к участку повреждённого сосуда. Кроме этого, фактор фон Виллебранда является транспортером фактора свёртывания крови VIII, стабилизирует его структуру, доставляет к месту повреждения и предупреждает потерю через почки.
Тромбоциты, роль в тромбоцитарно-сосудистом гемостазе
Тромбоциты или пластинки образуются в красном костном мозге гигантскими многоядерными клетками – мегакариоцитами, от цитоплазмы которых они отшнуровываются в виде округлых или овальных плоских дисков, диаметром от 2 до 4 мкм. Это безъядерные гранулоциты. Продолжительность жизни тромбоцитов человека составляет 7-10 дней.
После выхода из костного мозга они циркулируют в крови и частично депонируются в селезенке и печени (около 20-25% всех клеток), откуда происходит их вторичный выход в кровоток. В крови здоровых людей содержится 170-350х109/л тромбоцитов.
Уменьшение количества тромбоцитов до 80×109/л способствует появлению кровоточивости, риск которой резко возрастает при уровне тромбоцитов ниже 20×109/л, а увеличение выше 800×109/л создает угрозу развития тромбозов.
Участие тромбоцитов в тромбоцитарно-сосудистом гемостазе определяется следующими присущими им функциями:
- ангиотрофической – способностью поддерживать нормальную структуру и функцию стенок микрососудов, в том числе жизнеспособность и репарацию эндотелиальных клеток;
- способностью поддерживать спазм поврежденных сосудов путем секреции (высвобождения) вазоактивных веществ – серотонина, катехоламинов, содержащихся в плотных гранулах тромбоцитов;
- способностью образовывать в месте повреждения сосуда тромбоцитарную пробку, что обеспечивается процессами адгезии к субэндотелию отдельных тробоцитов и их агрегатов;
- участием тромбоцитарных факторов в процессе свертывания крови и регуляции фибринолиза;
- стимуляцией процесса репарации сосудистой стенки в месте ее повреждения фактором роста тромбоцитов (ФРТ) – цитокином, стимулирующим размножение и перемещение гладкомышечных клеток, клеток эндотелия и синтез коллагена.
В гиалоплазме тромбоцитов содержится два типа гранул (табл.1)
Таблица 1 – Компоненты гранул тромбоцитов, определяющих участие тромбоцитов в тромбоцитарно-сосудистом гемостазе
| δ-гранулы (электронно-плотные) | Альфа гранулы | |
| Компонент (Р) | Функция | |
| АДФ –активация тромбоцитов | Тромбоцитарный фактор роста | Репарация за счет активации деления фибробластов |
| Трансформирующий фактор роста β (ТФР-β) | Контроль репарация ткани | |
| Ca2+- активация тромбоцитов | Тромбоцитарный фактор 4 (ТФ-4) | Нейтрализация гепарина |
| Mg2+ –активация тромбоцитов | β-тромбоглобулин (β-ТГ) | Воспаление, репарация ткани |
| Фактор Виллебранда (ФВ) | Адгезия тромбоцитов, носитель ф.VIII | |
| Тромбоспондины (TSP-l, TSP- 2)* | Адгезия и агрегация тромбоцитов | |
| Серотонин –дилатация артериол | Фибриноген | Свертывание крови, адгезия и агрегация тромбоцитов |
| Фактор V | Свертывание | |
| Адреналин – спазм поврежденного сосуда | Протеин S | Антикоагулянт |
| ДОФА спазм поврежденного сосуда | ||
| Альбумин | Связывание гормонов, токсинов, лекарств | |
| Иммуноглобулины | Иммунитет |
*Тромбоспондин (TSP-l) – гликопротеид с м.м. 165 кДа. Наибольшее количество TSP-1 представлено в α-гранулах тромбоцитов и секретируется в плазму в ответ на их активацию гормонами и цитокинами.
Известно множество биологических реакций, инициируемых TSP-1: ангиогенез, апоптоз, регуляция иммунного ответа. TSP-1 образует комплексы с коллагеном, гепарином, опосредует адгезию тромбоцитов к субэндотелию.
Тромбоспондин-2 (TSP-2) – белок семейства тромбоспондинов с м.м. 150 кДа.
Аналогично TSP-1, он вызывает множество биологических реакций: пролиферацию, агрегацию, клеточную подвижность, ангиогенез, заживление ран.
TSP-2 регулирует формирование коллагенового матрикса, воздействуя на функцию фибробластов. Также TSP-2 обеспечивает взаимодействие клеток с экстрацеллюлярным матриксом, что можно отнести к его основной функции.
Из всех перечисленных факторов специфическими для гранул тромбоцитов являются два: ТФ4 – антигепариновый фактор и тромбоглобулин, определение которых в плазме крови используют как ранние надежные маркеры активации тромбоцитов.
Регуляция функций тромбоцитов осуществляется, как и всех клеток организма, путем взаимодействия регуляторных молекул (лигандов) с рецепторами их мембран – гликопротеинами (табл. 2).
Таблица 2 – Рецепторы тромбоцитов и их лиганды
| Гликопротеин | Лиганды | |
| Первичные | Вторичные | |
| GP IIb-IIIa | Фибриноген | Фактор Виллебранда, фибронектин, витронектин, фибриноген |
| GP Ib-IX | Фактор Виллебранда | Тромбин |
| GP Ia-IIa | Коллаген | |
| GP Ic-IIa | Фибронектин* | |
| Рецептор витронектина | Витронектин** | Тромбосподин |
*Фибронектин (ФН) – гликопротеин с высокой м.м., состоящий из двух практически идентичных полипептидных цепей (каждая по 220 кДа).
Он синтезируется и секретируется печенью, нормальная концентрация циркулирующего ФН в кровотоке составляет примерно 330 мкг/мл плазмы. ФН принадлежит к семейству адгезивных белков внеклеточного матрикса.
Димерная структура позволяет ему функционировать как молекулярный клей, соединяющий различные молекулы. Плазменный ФН выполняет важную роль в воспалительных, регенеративных процессах и механизмах гемостаза.
**Витронектин (ВН) – полифункциональный гликопротеин (м.м. 78 кДа), компонент крови и внеклеточного матрикса, выполняет функции аналогичные ФН. ВН синтезируется в печени, нормальная концентрация в плазме составляет 250-450 мкг/мл. ВН взаимодействует с комплементом, гепарином, комплексом тромбин-антитромбин.
Физиологическая активация тромбоцитов
Физиологическая активация тромбоцитов инициируется только при повреждении сосудистого эндотелия и обнажении субэндотелиального внеклеточного матрикса.
Первой в тромбоцитарно-сосудистом гемостазе инициируется адгезия тромбоцитов. С рецептором GP Ib-IX специфически связывается фактор Виллебранда, который вторым участком связывается с GP IIb-IIIa тромбоцитарной мембраны. Субэндотелиальный коллаген связывается с мембранным рецептором тромбоцитов GP Ia-IIa.
Адгезия инициирует активацию тромбоцитов, которая проявляется в существенном изменении их формы, необратимой дегрануляции α-гранул, агрегации тромбоцитов с образованием гемостатической тромбоцитарной пробки.
Активация тромбоцитов приводит к конформационному изменению рецептора GP IIb-IIIa, с которым связывается фибриноген и образует мостики между тромбоцитами, формируя агрегаты.
В мембранах активированных тромбоцитах из арахидоновой кислоты синтезируется и поступает в микроокружение тромбоксан А2 и фактор активации тромбоцитов (ФАТ). Оба соединения являются мощными активаторами тромбоцитов и их агрегации.
Освобождаемые из альфа гранул факторы свертывания крови определяют локальное образование тромбина и формирование нитей фибрина на поверхности агрегатов адгезированных тромбоцитов. Так формируется тромбоцитарный или первичный тромб. Процесс формирования первичного тромба, пробки в месте повреждения сосуда, занимает промежуток времени от З0 секунд до З минут.
В условиях нормы процесс “установки заплат“ на сосудах микроциркуляторного русла осуществляется постоянно, но маркеры активации тромбоцитарно-сосудистого гемостаза в кровотоке не определяются, так как этот процесс имеет локальный характер, обусловленный нейтрализующим действием антикоагулянтных факторов здорового эндотелия.
Мембраны активированных тромбоцитов, пластиночный фактор 3 (3пф), выполняет функцию фосфолипидной матрицы, обязательной составляющей молекулярной машины активации гуморальных факторов внутреннего и общего пути свертывания крови.
Тромбоциты обеспечивают поверхность для сборки и активация комплексов свертывания крови и генерации тромбина. Тромбин превращает фибриноген в фибрин.
Нити фибрина связывают агрегированные тромбоциты, обеспечивая формирование не смываемого током крови гемостатического тромба.
- Следовательно, в реализации тромбоцитарно-сосудистого гемостаза участвуют субэндотелий стенки сосудов, тромбоциты и гликопротеины плазмы, в том числе фибриноген и фактор Виллебранда, которые также представлены в тромбоцитах.
- В норме кровотечение из мелких сосудов прекращается не более чем через 5 минут.
- Нарушение в системе тромбоцитарно-сосудистого гемостаза проявляются петехиально-пятнистым типом кровоточивости и артериальными тромбозами.
Морфофункциональная характеристика тромбоцитов в норме и при патологии. Понятие о гемостазе. Тромбоцитарно-сосудистый гемостаз
Система
гемостаза – это
система механизмов, которые, с одной
стороны, поддерживают жидкое состояние
крови, с другой – обеспечивает закупорку
поврежденных сосудов и остановку
кровотечений.
Компоненты гемостаза
– их 3:
-
Сосудистая стенка,
-
Клетки крови (прежде всего тромбоциты),
-
Плазменные ферментные системы:
- — свертывающая,
-
— противосвертывающая
– тромбоциторезистентность сосудистой
стенки + система антикоагулянтов +
фибринолитическая (или плазминовая)
система. - Виды гемостаза:
-
Тромбоцитарно-сосудистый (первичный) гемостаз,
-
Коагуляционный (вторичный) гемостаз.
Тромбоцитарно-сосудистый гемостаз
Тромбоцитарно-сосудистый
гемостаз (ТСГ) первым реагирует на
повреждение – в связи с этим его называют
первичным. Компонентами ТСГ являются
сосудистая стенка и тромбоциты.
Происхождение и биологические свойства тромбоцитов
Схема образования
тромбоцитов:
мегакариобласт → промегакариоцит →
мегакариоцит → тромбоцит (в результате
отщепления от мегакариоцита).
Мегакариоцитопоэз
протекает в КМ. Отличительной его чертой
является деление клеточного ядра без
разделения цитоплазмы – в результате
из мегакариобласта небольших размеров
(18-20 мкм) образуются гигантские клетки — мегакариоциты диаметром 30-40 мкм
(мегакариоцит – самая крупная клетка
КМ).
Процесс созревания мегакариобласта
в мегакариоцит занимает около 25 ч.
Дифференцировка мегакариоцитов
происходит вблизи КМ-ых синусов. По мере
созревания внутрь мегакариоцита врастают
разделительные мембраны, происходит
деление цитоплазмы на тромбоциты.
Отшнуровка тромбоцитов происходит в
синусах КМ, куда проникают лентообразные
отростки цитоплазмы мегакариоцита.
Время созревания
тромбоцита – 8 дней, время пребывания
в кровотоке – 9-11 дней. Место гибели –
селезенка, печень, легкие. Нормальное
содержание тромбоцитов в крови – 150-350
Г/л. Выделяют 2 пула тромбоцитов:
циркулирующий (это примерно 67% клеток)
и пристеночный (оставшиеся 33%).
Тромбоциты –
безъядерные тельца со средним диаметром
2-4 мкм. Различают юные (незрелые) (2-4,5%),
зрелые (87-98%), старые тромбоциты (0-3%) и
формы раздражения (2-4,5%).
Кроме того
выделяют микро-, макро- и мегалоформы
тромбоцитов (их диаметр соответственно
составляет 1,5, 5 и 6-10 мкм). В цитоплазме
зрелого тромбоцита содержится обильная
азурофильная зернистость. Форма клеток
– круглая или овальная.
При активации
клетки образуют псевдоподии и приобретают
звездчатую форму. В структуре тромбоцита
выделяют 2 основные зоны:
-
Мембрана – богата фосфолипидами (на поверхности которых происходит взаимодействие плазменных факторов свертывания), имеет рецепторы:
— гликопротеины
I,
II,
III,
состоящие из 2-х субъединиц (α
и β)
– они необходимы для адгезии, агрегации,
ретракции сгустка и взаимодействия с
фибриногеном, фактором Виллебранда,
фибронектином,
— рецепторы для
адреналина, АДФ и др.
-
Гель-зона (матрикс цитоплазмы) – в ней располагаются:
-
— микротрубочки и
филаменты – они обеспечивают образование
псевдоподий, участвуют в секреции; -
— канальцы –
участвуют в секреции, -
— грануломер:
плотные тельца и α-гранулы – содержащиеся
в них вещества обладают вазоактивным
действием, опосредуют активацию, адгезию
и агрегацию тромбоцитов, обеспечивают
ретракцию тромба.
Плотные тельца
содержат пероксидазу, катионные белки
и небелковые компоненты (АМФ, АДФ, АТФ,
фибронектин, адреналин и норадреналин,
серотонин, гистамин, ионы Са2+
и т.д).
В состав α-гранул
входят
фибриноген, фактор Виллебранда,
тромбоспондин, фибронектин, β-тромбоглобулин,
тканевой активатор плазминогена (t-pa),
IV
и V
факторы свертывания, фибринстабилизирующий
фактор, фактор роста тромбоцитов,
калликреин, α2-антиплазмин
и др., а также гликоген и гидролитические
ферменты (кислая фосфатаза, неспецифическая
эстераза, β-глюкуронидаза, катепсины).
Функции
тромбоцитов:
-
Ангиотрофическая – поддерживают целостность и нормальную проницаемость сосудистой стенки, способствуют её репарации (реэндотелизации). На эту функцию ежедневно расходуется около 15% циркулирующих тромбоцитов.
-
Вазоконстрикторная (ангиоспастическая) – тромбоциты высвобождают вазоактивные вещества — адреналин, норадреналин, серотонин, ТхА2.
-
Закупорка поврежденных сосудов – обусловливается способностью тромбоцитов прилипать к субэндотелиальным структурам поврежденной сосудистой стенки (адгезия), образовывать скопления (агрегация), вызывать ретракцию кровяного сгустка с образованием первичного тромба (посредством секреции тромбостенина, который осаждается на нитях фибрина и вызывает их уплотнение и скручивание).
-
Активация коагуляционного гемостазаза счет тромбоцитарных фак-
-
Участие в воспалении торов, освобождающихся при
дегрануляции
тромбоцитов.
-
Сорбционно-транспортная – состоит в адсорбции тромбоцитами на своей поверхности и доствке к месту кровотечения плазменных факторов свертывания, антикоагулянтов, БАВ (например, серотонина), ЦИК.
-
Защитная – тромбоциты способны фагоцитировать чужеродные частицы, вирусы и АТ (выражена слабо).
Сосудисто-тромбоцитарный (первичный) гемостаз. Общая информация
Остановка кровотечения при повреждении стенки сосуда начинается с сосудистотромбоцитарных реакций. Основным звеном первичного гемостаза являются тромбоциты. Плазматическая мембрана тромбоцитов имеет двухслойную структуру, ее продолжением служит открытая канальцевая система, связанная с поверхностью клетки.
В этой системе канальцев секретируется содержимое внутритромбоцитарных гранул. Плотные гранулы секретируют низкомолекулярные вещества – ионы кальция, серотонин, АТФ, АДФ. Высокомолекулярные соединения (тромбоцитарные факторы, фактор Виллебранда, ростовые факторы, тромбоглобулины и др.) секретируются α-гранулами.
Также тромбоциты секретируют кислые гидролазы, ряд белков и липидов, которые играют важную роль в первичном гемостазе.
Тромбоциты способны к быстрой адгезии почти ко всем известным искусственным и естественным поверхностям: стеклу, в т. ч. и покрытому силиконом, коллагену, эластину, мембране фибробластов и др.
В норме тромбоциты циркулируют в крови, не прикрепляясь к эндотелию.
При повреждении эндотелиальной выстилки сосудов в тромбоцитах происходят морфологические и метаболические изменения, способствующие адгезии к субэндотелию, агрегации и реакции высвобождения биологически активных веществ.
Вещества, выделяемые тромбоцитами, вызывают разнообразные эффекты: стимулируют спазм сосудов, адгезию и агрегацию тромбоцитов, а также плазменный гемостаз.
Тромбоцитарный и другие факторы роста стимулируют миграцию и пролиферацию гладкомышечных клеток и фибробластов, ингибируют миграцию и пролиферацию эндотелиальных клеток.
Другие выделяемые кровяными пластинками вещества повышают проницаемость сосудов, связывают гликозаминогликаны, индуцируют хемотаксис лейкоцитов к месту повреждения сосуда.
Одновременно с адгезией происходит образование агрегатов, обусловленное воздействием на тромбоциты биологически активных веществ: АДФ, адреналина, тромбина и др. Регуляторами агрегации тромбоцитов являются концентрация ионов кальция в тромбоцитах и уровень циклических нуклеотидов.
Во взаимодействии тромбоцитов с сосудистой стенкой важная роль принадлежит адгезивным гликопротеинам, которые содержатся в плазме, тромбоцитах и сосудистой стенке. К ним относятся фибриноген, витронектин, фибронектин, фактор Виллебранда и др.
Растворимый фибриноген после соединения со специфическими рецепторами на поверхности тромбоцитов и сосудистой стенки подвергается конформационным изменениям и образует вокруг кровяных пластинок плотные аморфные или пластинчатые структуры, которые служат высококонцентрированным суб-стратом для тромбина.
Активированные тромбоциты представляют каталитическую поверхность для активации сериновых протеаз коагуляционного каскада и быстрой генерации тромбина.
Последний отщепляет от фибриногена фибринопептид, индуцирует дальнейшую многоступенчатую полимеризацию и образование нерастворимого сгустка, который представляет собой трехмерную тромбино-фибриновую сеть с расположенными в узловых ее точках тромбоцитами или их агрегатами. Укрепление фибриновых волокон достигается также образованием ковалентных поперечных связей с помощью фактора XIIIa.
Первичный гемостатический тромб нестабилен и проницаем для жидкой части крови. Одновременно с сосудисто-тромбоцитарным гемостазом включается и коагуляционный (плазменный) гемостаз за счет активации факторов свертывания крови, адсорбированных на поверхности тромбоцитов.
Сосудисто-тромбоцитарный гемостаз
7471
Биологическая система, обеспечивающая, с одной стороны, предупреждение и купирование кровотечений, а с другой — сохранение жидкого состояния крови, называется системой гемостаза. По мнению О. Г. Гаврилова, эта система является частью более сложной многокомпонентной системы регуляции агрегатного состояния крови (PACK).
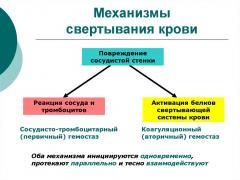
В осуществлении гемостаза принимают участие три взаимодействующих между собой функционально-структурных компонента: стенки кровеносных сосудов, клетки крови (в первую очередь, тромбоциты) и плазменные ферментные системы — свертывающая, противосвертывающая, фибринолитическая или плазминовая, калликреин-кининовая и система комплемента.
Особенно тесно связаны между собой внутренняя оболочка сосудов и тромбоциты. Их объединяют в общий сосудисто-тромбоцитарный или первичный гемостаз.
Микрососудам (диаметр до 100 мкм) и тромбоцитам принадлежит ведущая роль в остановке кровотечений в зоне микроциркуляции, тогда как образование фибрина происходит несколько позже и обозначается как вторичный или коагуляционный гемостаз.
Неповрежденный эндотелий сосудистой стенки обладает свойством тромборезистентности и играет важную роль в сохранении жидкого состояния крови. Это свойство определяется следующими качествами эндотелия:
- способностью образовывать и выделять в кровь простациклин (метаболит арахидоновой кислоты, относящийся к простагландинам) и эндотелиальный фактор релаксации (ЭФР/NO) — мощные ингибиторы агрегации тромбоцитов с вазодилятирующими свойствами;
- предупреждением контактной активации системы свертывания крови. Эндотелий участвует в элиминации фIХа из кровотока: после присоединения к рецепторам эндотелия фIХа образует комплекс с антитромбином-III (AT-III); наиболее интенсивно этот процесс происходит в легких. Затем комплекс отрывается от клетки и удаляется из крови гепатоцитами;
- контакт с эндотелиоцитами в 19 раз ускоряет реакцию между тромбином и AT-III, что обеспечивается гепариноподобными соединениями на эндотелии;
- тромбомодулин — один из рецепторов эндотелиоцитов — образует с тромбином комплекс, который активирует протеин С и одновременно теряет способность свертывать фибриноген.
Предполагается, что фибриновый слой постоянно образуется на эндотелии. Наличие его обеспечивает нормальное функционирование эндотелия, проницаемость и резистентность сосудистой стенки.
Участие эндотелия в фибринолитических процессах определяется содержанием в сосудистой стенке активатора плазминогена.
Небольшие порции его постоянно выделяются из эндотелия и вместе с другими протеазами обеспечивают «пристеночный» фибринолиз; эндотелиоциты продуцируют также ингибитор активатора плазминогена; в эндотелии синтезируется фХII, который через высокомолекулярный кининоген запускает «хагеманзависимый» фибринолиз.
Вместе с тем, стенка сосуда в силу своих анатомо-физиологических свойств (ригидности, эластичности, пластичности) способна противостоять как давлению крови, так и внешнему травмирующему воздействию и тем препятствует возникновению геморрагии.
Это свойство зависит от полноценности эндотелия и от особенности строения субэндотелиального слоя: качества коллагена, соотношения коллагеновых и эластичных волокон, структуры базальной мембраны и т. д.
Монослой эндотелиоцитов поставляет в субэндотелий ряд веществ: компоненты базальной мембраны, коллаген, эластин, ламилин, протеазы и их ингибиторы, тромбоспондин, мукополисахариды, витронектин, фибронектин и фактор Виллебранда.
Эти белки обеспечивают межклеточные взаимодействия и образование диффузионного барьера, который предотвращает попадание крови из внутрисосудистого пространства во внесосудистое.
Проницаемость сосудистой стенки зависит во многом от количества и качества тромбоцитов.
Уменьшение содержания тромбоцитов или изменение их свойств приводит к нарушению их ангиотрофической функции, а это, в свою очередь, к повышению проницаемости и ломкости микрососудов, к появлению петехиально-пятнистого (или микрососудистого) типа кровоточивости. Становятся положительными пробы на ломкость сосудов, легко возникают петехии, синячки, кровотечения из слизистых.
После стимуляции или травмы эндотелий с обнажившимся субэндотелиальным слоем трансформируется в мощную прокоагулянтную поверхность. Это обеспечивается синтезом, выделением или привлечением многих прокоагулянтов:
- секрецией фактора активирующего тромбоциты (ФАТ), который обуславливает адгезию тромбоцитов на эндотелии; стимулятора агрегации тромбоцитов — тромбоксана (ТхА2);
- продукцией тканевого фактора — тромбопластина (осуществляющейся с участием арахидоновой кислоты, цАМФ, Са++);
- эндотелий регулирует содержание компонентов калликреин-кининовой системы;
- эндотелиоциты секретируют факторы свертывания (фV, фVIII), антиген фVIII, фактор Виллебранда, ингибитор активатора плазминогена (ИАП-1 и ИАП-2), интерлейкин-1, фактор некроза ткани, вазоконстрикторы — эндотелии-1, адреналин, норадреналин, АДФ.
При нарушении целостности сосуда первой реакцией является его спазм в месте повреждения, что способствует остановке кровотечения, и расширение его выше места травмы, что способствует открытию шунтов выше места повреждения.
Этим достигается снабжение кровью тканей ниже места повреждения.
Вазоконстрикция как реакция на травму (длительностью менее 60 секунд) приводит к снижению кровотока, что улучшает взаимодействия между тромбоцитами, факторами свертывания крови и поврежденным участком.
Происходит контактная активация коллагеном и другими компонентами субэндотелия тромбоцитов в месте повреждения и фXII плазмы (фактора контакта), в результате чего активируется адгезия тромбоцитов в месте повреждения и начинается активация системы свертывания по внутреннему пути. Таким образом, стен¬ка сосуда связана со всеми другими звеньями системы гемостаза, особенно с тромбоцитами.
- Участие тромбоцитов в гемостазе определяется в основном следующими их функциями:
- 1) ангиотрофической;
- 2) способностью поддерживать спазм поврежденного сосуда путем секреции вазоактивных веществ (в результате реакции освобождения) — адреналина, норадреналина, серотонина и др.;
- 3) способностью образовывать первичный тромб с помощью адгезивности и агрегационной функции;
- 4) способностью выделять гемостатические факторы — тромбопластическая способность.
Ведущая роль в осуществлении первичного гемостаза принадлежит адгезивно-агрегационной функции тромбоцитов. Пусковой момент в этом процессе — повреждение сосудистой стенки и контакт тромбоцитов с субэндотелием.
Это приводит к активации тромбоцитов. Активация тромбоцитов происходит в 3 этапа:
I. Индукция — воздействие серотонина, АДФ, коллагена, тромбина, адреналина, простагландинов (Pg), тромбоксана.
II.
Трансмиссия — высвобождение из депо Са++ в плазму и снижение уровня цАМФ: происходят контрактильные реакции, тромбоциты меняют форму; при стимуляции фосфолипазы образуются Pg, ФАТ, происходит адгезия (распластывание) с участием фактора Виллебранда (фW) и фибронектина. Усиливает агрегацию гликопротеид тромбоспондин, содержащийся в α-гранулах тромбоцитов и тромбоксан А2, ингибирует — простациклин, ТФР (тромбоцитарный фактор роста), оксид азота.
III.
Реакция высвобождения: при действии слабых активаторов (АДФ, серотонина) — выделяется АДФ, АТФ, Са++, Mg++, серотонин, гистамин, дофамин; под действием тромбоксана, арахидоновой кислоты, иммунных комплексов — выделяется ф4, фибриноген, фW, фVIII, фV, антиплазмин, ТФР, тромбоспондин, фибронектин, ингибитор активатора плазминогена и т. д. (реакция освобождения-I); высокие концентрации тромбина вызывают секрецию лизосомальных ферментов (реакция освобождения-II).
Наряду с адгезией идет процесс агрегации тромбоцитов — склеивание их между собой и образование первичной тромбоцитарной пробки. Этот процесс стимулируется АДФ, выделяемой из гемолизирующихся в зоне повреждения эритроцитов, а также катехоламинами и серотонином. Гемостатическая пробка быстро увеличивается в объеме и через 1-3 минуты полностью закрывает просвет кровоточащего сосуда.
Важную роль в регуляции тромбоцитарного гемостаза играют производные арахидоновой кислоты, освобождаемой из мембранных фосфолипидов тромбоцитов и стенки сосудов вследствие активации фосфолипаз.
В дальнейшем под влиянием циклооксигеназы из арахидоновой кислоты образуются простагландины, а из них в тромбоцитах под влиянием тромбоксансинтетазы вырабатывается чрезвычайно мощный агрегирующий агент тромбоксан-А2 (ТхА2), а в стенке сосудов под влиянием простациклинсинтетазы — основной ингибитор агрегации простациклин (простагландин I2 —PgI2).
Изменение иммунного статуса организма отражается на функциональной активности тромбоцитов. Иммунные комплексы приводят к тромбозам даже при интактной системе комплемента за счет стимуляции тромбоцитов.
Один из вариантов — HELLP-синдром при тяжелых гестозах. На поверхности тромбоцитов оседают антитела и иммунные комплексы, вызывающие деструкцию с последующим фагоцитозом системой мононуклеарных макрофагов.
При РДСВ происходит «захват» тромбоцитов, которые становятся медиаторами дальнейшего повреждения (в бронхо-альвеолярном секрете обнаруживают тромбоциты, тромбопластин, микроэмболы, фибриновые тромбы, коллагеновые волокна, РКМФ, продукты деградации фибрина).
В результате воздействия тромбоцитарных и плазменных факторов в зоне гемостаза образуется тромбин, малые дозы которого усиливают и завершают процесс миграции и одновременно вызывают свертывание крови, в силу чего тромбоцитарная пробка покрывается фибрином и подвергается уплотнению (ретракции) с помощью сократительного белка — тромбостенина.
Помимо перечисленных выше агентов, в тромбоцитах и в других клетках крови образуются другие мощные стимуляторы агрегации. Из них в последние годы большое внимание уделяется фосфолипидному пластиночному агрегирующему фактору (PAF) из лейкоцитов и тромбоцитов.
Кроме того, в лейкоцитах содержится прокоагулянт (фЗ тромбоцитов), аналоги плазменных факторов свертывания крови, антикоагулянты, стимуляторы и ингибиторы фибринолиза.
Существенные изменения прокоагулянтной и фибринолитической активности лейкоцитов возникают при ряде ситуаций, когда меняется иммунный статус организма.
При этом лейкоцитам отводится ведущая роль в патогенезе ДВС-синдрома.
С одной стороны, лейкоциты активируют контактную фазу коагуляции, т.к. содержат киназы и ферменты, стимулирующие кининогенез, с другой стороны, некоторые протеазы нейтрофилов значительно тормозят процесс свертывания.
Лейкоциты разрушают фибрин путем механического, фагоцитарного, химического тромболизиса и лейкофибринолиза при помощи фибринолитических протеаз. Хемотаксическая активность лейкоцитов генерируется фIIа, фХIIа, ПДФ, кининогенином, активатором плазминогена.
Таким образом, лейкоциты одновременно стимулируют сосудисто-тромбоцитарный гемостаз через простагландины, свертывание крови и фибринолиз — через фХН, сосудистый тонус через кининовую систему (Б. И. Кузник, 1984).
Эритроциты содержат аналог фЗ тромбоцитов, антигепариновый ф4, АДФ, активатор плазминогена, антиплазмин. Кроме того, при различных патологических процессах нарушается «способность эритроцитов к деформации», обуславливающая дальнейшие нарушения микроциркуляции и гемостаза.
Макрофаги вырабатывают прокоагулянт со свойствами тромбопластина. Индукторами в этой реакции являются Т-лимфоциты, предварительно обработанные иммунными комплексами или IgG, они выделяют лимфокины, усиливающие образование моноцитами прокоагулянта.
Моноциты в присутствии иммунных комплексов и липополисахаридов способны синтезировать протромбиназу, витамин-К-зависимые факторы (II,VII,IX,X), фибриназу.
При определенных условиях макрофаги выделяют в окружающую среду кислые гидралазы, компоненты комплемента, протеазы, активатор плазминогена, регулирующие фибринолитическую активность.
В зависимости от вида антигена стимулированные лимфоциты индуцируют синтез макрофагами или активатора плазминогена или ингибиторов фибринолиза. Макрофаги продуцируют ФАТ в процессе фагоцитоза иммунных комплексов.
Базофилы содержат соединения, влияющие на состояние системы гемостаза: гепарин, гистамин, серотонин, ФАТ, активатор плазминогена, стимулятор кининовой системы, эозинофильный хемотаксический фактор и др.
В физиологических условиях происходит выделение небольших количеств медиаторов, необходимых для поддержания гемостаза.
При дегрануляции под действием биологически активных веществ эти соединения проявляют свою активность как местно, так и в общем кровотоке.
Первичной тромбоцитарной пробки, образовавшейся в результате активации сосудисто-тромбоцитарного компонента гемостаза, достаточно для того, чтобы начался процесс свертывания. Но постоянная гемостатическая пробка формируется при образовании тромбина, вызывающего необратимую агрегацию тромбоцитов и отложение фибрина на тромбоцитарных агрегатах в месте сосудистой травмы.
Лысенков С.П., Мясникова В.В., Пономарев В.В.
Неотложные состояния и анестезия в акушерстве. Клиническая патофизиология и фармакотерапия
Опубликовал Константин Моканов
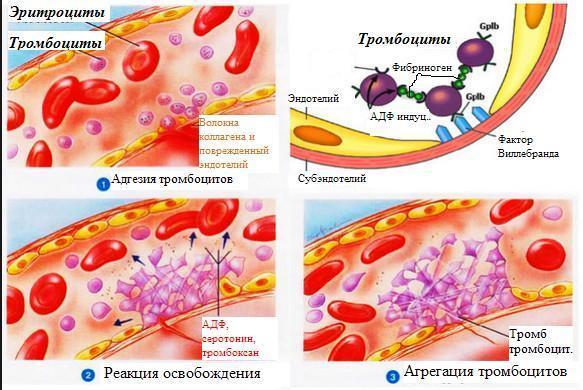 в месте повреждения сосуда реализуется следующая последовательность реакций (рис.). Во-первых, тромбоциты прилипают (адгезируют) к открытому субэндотелиальному слою коллагена. Прилипанию тромбоцитов предшествует изменение их формы: клетки поврежденной ткани освобождают АДФ — мощный активатор тромбоцитов. Во-вторых, активированные тромбоциты освобождают ряд соединений в том числе аденозиндифосфат (AДФ). Освобожденный АДФ стимулирует другие тромбоциты к адгезии в ране, и, в-третьих, происходит, агрегация активированных тромбоцитов. При агрегации тромбоциты прилипают друг к другу и инициируют начало образования тромба. Наконец, в месте повреждения активируются белки свертывания крови, образуется фермент тромбин, который превращает растворимый белок свертывания фибриноген в нерастворимые нити фибрина, нити армируют агрегаты тромбоцитов и заканчивают формирование белого тромбоцитарного тромба.
в месте повреждения сосуда реализуется следующая последовательность реакций (рис.). Во-первых, тромбоциты прилипают (адгезируют) к открытому субэндотелиальному слою коллагена. Прилипанию тромбоцитов предшествует изменение их формы: клетки поврежденной ткани освобождают АДФ — мощный активатор тромбоцитов. Во-вторых, активированные тромбоциты освобождают ряд соединений в том числе аденозиндифосфат (AДФ). Освобожденный АДФ стимулирует другие тромбоциты к адгезии в ране, и, в-третьих, происходит, агрегация активированных тромбоцитов. При агрегации тромбоциты прилипают друг к другу и инициируют начало образования тромба. Наконец, в месте повреждения активируются белки свертывания крови, образуется фермент тромбин, который превращает растворимый белок свертывания фибриноген в нерастворимые нити фибрина, нити армируют агрегаты тромбоцитов и заканчивают формирование белого тромбоцитарного тромба.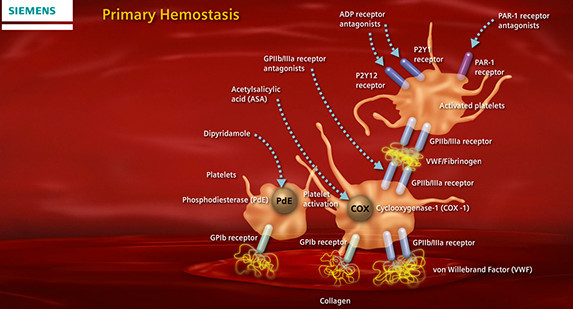 Физиологическая активация тромбоцитов инициируется только при повреждении сосудистого эндотелия и обнажении субэндотелиального внеклеточного матрикса.
Физиологическая активация тромбоцитов инициируется только при повреждении сосудистого эндотелия и обнажении субэндотелиального внеклеточного матрикса.